Смешные лица картинки (45 фото) 🔥 Прикольные картинки и юмор
Людям всегда весело, когда другие попадают в смешные и нестандартные ситуации. Веселые фото поднимают настроение и улучшают самочувствие. Поэтому дальше смотрим картинки смешных лиц людей.

Бывают же … смешные люди!

Стильная бабулька)

Наш любимый Мистер Бин!

Прикольная карикатура на Уилл Смита!

Одно лицо)))

Фото детей всегда самые смешные!

Может … хочет, что-то сказать?

Это тот случай, когда лицо не важно!

Задумался, наверное…

Ну и рожа)

Собаки всегда похожи на своих хозяев!

Сейчас забью…

Смешной ботаник)

Можешь и не стараться!

Умный мальчик)

Хи-хи-хи…


Креативненько!

Вдох … выдох…

Милая … девчушка)

Рыжий конопатый убил дедушку…

Стильная челка!

Чем-то недовольны!

Я … тебя порву…

Осторожно! Мяч! Наверное, думают чем отбить?


Джордж Клуни хочет соблазнить девушку!

А … откушу….

Смешной солдатик)

Хочет напугать быка!

Смешные свидетели, наверное, что-то натворили… или невеста страшненькая)

А вы … так умеете?

Чего ты радуешься!

Милые дворовые ребята)))

Аааа … что сказать….

Ровные зубки)

Уууу … аааа…

Умный профессор!

Любимый Сергей Юрьевич Беляков, который любит разговаривать с телевизором….

На язык краски не хватило)

Стиляга!

Вколол себе ботокс в губки)

Специально сделала себе грудь, чтоб отвернуть внимание от лица)

Мужчина — хомяк)

Мне нравится7Не нравится2
Будь человеком, проголосуй за пост!
 Загрузка…
Загрузка…
Смешные лица (45 фото)
Из последних комментариев на сайте я сделала вывод, что мне вообще больше не стоит про себя что-то рассказывать. Что бы я не написала, обязательно всё переиначат, найдут двойной-тройной смысл слов, обзовут неприличными словами и т.д.. Так что вот вам прикольные рожи парней и девушек. А теперь думайте сами, что они означают и почему я собрала приколы именно на эту тему.












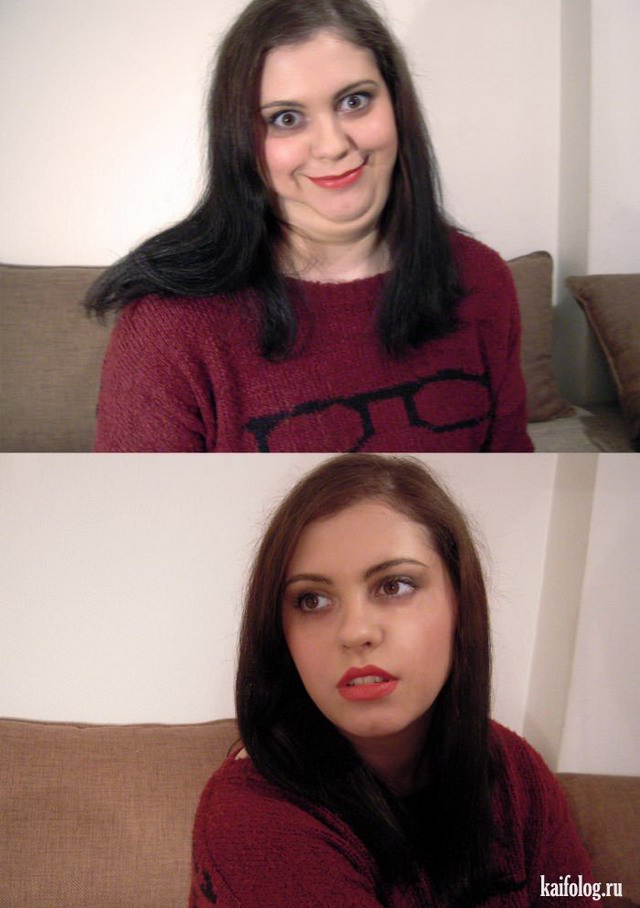
































Смешные лица людей — прикольные картинки (40 фото) • Прикольные картинки и позитив
Предлагаем улыбнуться прямо сейчас, ведь смешные лица людей на фото помогут вам рассмеяться. Прикольные картинки человеческих лиц в момент удивления или других ситуаций улучшат ваше самочувствие до максимума.Лица теннисистов во время игры.Жрет майку.
Смешные лица политиков.
Лицо прикольной девушки.
Лица странных людей.
Прикольная картинка с мужчиной.
Прическа Обамы.
Страшный грузин.
Смешная картинка с лицом девушки.
Щеки парня лопнут.
Смещная женщина на фото.
Лицо темнокожего парня.
Смешные усы.
Длинный язык.
Прикольное лицо Белякова.
Мультяшная картинка.
Удивленные лица людей.
Прикол на картинке.
Джим Керри и его лицо.
Беззубые алкаши.
Еще один алкоголик.
Смешная улыбка парня.
Азиат кусает соперника.
Лицо женщины.
Страшилище.
Милые лица девушек.
Красивая девушка.
Толстое лицо тетки.
Толстяк.
Мелкий ребенок.
Смешное лицо девушки.
Лицо футболиста возле мяча.
Пес и девушка.
Старик противный.
Смешной парень.
Удивленная бодибилдерша.
Малыш и его смешное лицо.
Лицо прикольной девушки.
Самые смешные рожи (37 фото)
Кто из нас никогда не гримасничал и не делал смешные рожи? Многие делали, знаю. И так, люди, у которых это получается лучше всех и не специально. 🙂















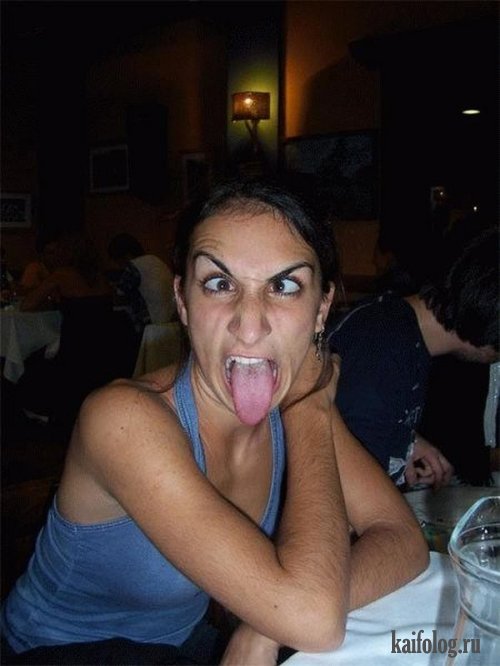









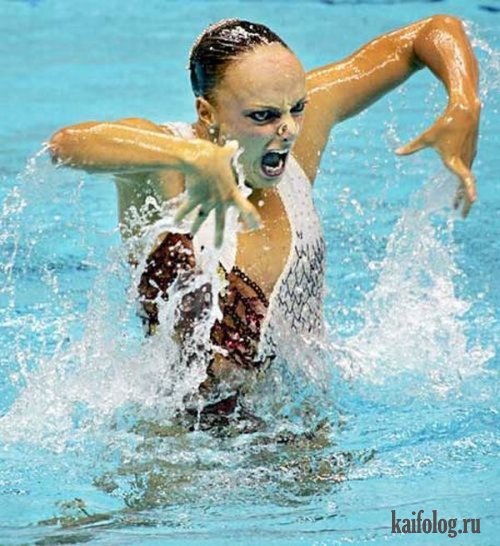






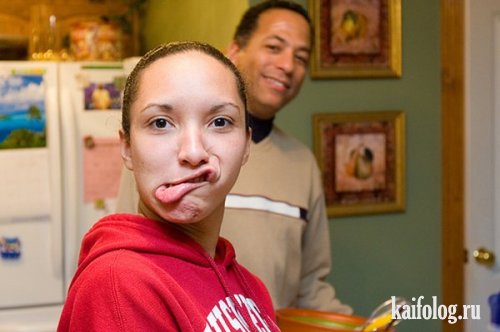



Самые смешные лица людей (18 фото)
Главная / Юмор / Самые смешные лица людей (18 фото)Вы и сами наверняка замечали, что на фотографиях наши лица порой получаются не совсем такими, какими мы привыкли видеть их в зеркале. Фотография имеет одну интересную особенность. Она беспристрастно фиксирует всё, что происходит в доли секунды. Фотокамере абсолютно всё равно, как выглядит человек, в какой он позе заходится, что происходит с его лицом и так далее. Больше того, на кадр попадают такие мельчайшие подробности, которые из-за своей скоротечности зачастую просто не улавливаются глазом. В итоге мы можем обнаружить на фотографиях такие моменты, зачастую очень смешные, которые просто не смогли увидеть в момент съёмки.
Здесь вы можете увидеть подборку из 18 фотографий с самыми смешными лицами людей. Фотографии имеют самый разный характер. Одни созданы специально, когда люди корчили гримасы, чтобы насмешить других людей. Другие были сделаны случайно, когда наверное никто даже не предполагал, что на снимке люди предстанут настолько смешными и забавными. Также здесь представлены фотографии спортсменов, которые в напряжённый момент игры или каких-либо действий в последнюю очередь задумываются над тем, как выглядит их лицо. Во всяком случае, фотографии очень смешные и могут поднять вам настроение.
Если вы хотите поделиться своими смешными фотографиями, то оставляйте их вместе со своими сообщениями в комментариях.
Самые смешные лица людей фото



















Необходима качественная реклама на билбордах Москвы и МО? Узнайте всё об услугах и расценках на сайте рекламного агентства «Мастер». Билборды, ситиборды, вывески, объёмные буквы, световые короба и многое другое.

По теме: Трещётка
👤 Блинцов | 2017-10-03, 12:34
20 смешных лиц, которые люди увидели в повседневных предметах
Для тех, кто постоянно видит лица в окружающих предметах, облаках, еде и тому подобном придумали термин, описывающий их состояние, и назвали его парейдолия. А если вы не понимаете, о чём идёт речь, то вспомните хотя бы лицо печального человека, которого все видят глядя на луну — классический пример парейдолии. Предлагаем вам взглянуть на забавные примеры этих зрительных иллюзий, которые окружают нас в повседневной жизни.
Снупи в кофе
Злорадная пара обуви
Фигура женщины в апельсине
Брат, это ты?
Разъярённая курица
[region:bone:inline_1]
Оливка, ты пьяна, иди домой
Отражение черепах похоже на бородатых мужчин
«Птица нагадила на лобовое стекло моей машины и из этого получился голубь»
Это же Коржик!
Грустный чемодан
[region:bone:inline_2]
Подозревающий вампир
Кактус, взбирающийся по скале
Удивлённая пальма
«Я нашёл этого парня за фоторамкой»
«Руки вверх»
[region:bone:inline_3]
«Я упал и не могу подняться!»
Счастливый снег
Огненный монстр
«Нет, только не это!»
«Я разбил яйца на сковороду, а из них вылетело приведение»
Поделиться в соц. сетях
Окись углерода — Простая английская Википедия, бесплатная энциклопедия
[1]| Имена | |||
|---|---|---|---|
| Предпочтительное название IUPAC | |||
| Прочие наименования Оксид углерода | |||
| Идентификаторы | |||
| Beilstein Ссылка | 3587264 | ||
| ЧЭБИ | |||
| ChemSpider | |||
| ECHA InfoCard | 100.010.118 | ||
| Номер ЕС | 211-128-3 | ||
| Gmelin Артикул | 421 | ||
| КЕГГ | |||
| МеШ | {{{value}}} | ||
| PubChem | {{{value}}} | ||
| Номер RTECS | FG3500000 | ||
| UNII | |||
| Номер ООН | 1016 | ||
| УЛЫБКИ | {{{value}}} | ||
| Недвижимость | |||
| CO | |||
| Молярная масса | 28.010 г / моль | ||
| Внешний вид | бесцветный газ | ||
| Запах | без запаха | ||
| Плотность | 789 кг / м 3 , жидкость 1,250 кг / м 3 при 0 ° C, 1 атм 1,145 кг / м 3 при 25 ° C, 1 атм | ||
| Температура плавления | -205,02 ° С (-337,04 ° F, 68,13 К) | ||
| Температура кипения | |||
| 27.6 мг / л (25 ° С) | |||
| Растворимость | растворим в хлороформе, уксусной кислоте, этилацетате, этаноле, гидроксиде аммония, бензоле. | ||
| к H | 1,04 атм · м 3 / моль | ||
| −9,8 · 10 −6 см 3 / моль | |||
| 1.0003364 | |||
| 0,122 D | |||
| Термохимия | |||
| Стандартная энтальпия образования Δ f H | -110.5 кДж / моль | ||
Δ c H | -283,4 кДж / моль | ||
| Стандартная молярная энтропия S | 197,7 Дж / (моль · К) | ||
| Удельная теплоемкость, С | 29,1 Дж / (К · моль) | ||
| Опасности | |||
| Классификация ЕС | Факс: + Тел .: + | ||
| NFPA 704 | 4 3 0 | ||
| R-фразы | | ||
| S-фразы | S53 S45 | ||
| Пределы взрываемости | 12.5–74,2% | ||
| Допустимый предел воздействия США (PEL) | TWA 50 частей на миллион (55 мг / м 3 | ||
| Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |||
| Y проверить (что такое YN ?) | |||
| Ссылки на инфобокс | |||
Окись углерода с химической формулой CO — это бесцветный газ без запаха и вкуса.Он состоит из одного атома углерода, ковалентно связанного с одним атомом кислорода. Он образуется при горении углеродных соединений и недостатке кислорода. Это хорошее топливо, оно горит на воздухе голубым пламенем, образуя углекислый газ. Он очень токсичен, но полезен и для современной техники.
Наиболее важным применением окиси углерода в промышленности является производство железа из железной руды. Окись углерода забирает кислород из железной руды при нагревании в большой печи, называемой доменной печью. Жидкое железо осталось позади.Окись углерода превращается в двуокись углерода.
Окись углерода может случайно образоваться, когда воздуха слишком мало, чтобы сжечь все топливо до двуокиси углерода. Такая ситуация может произойти, если жалюзи духовки закрываются слишком рано или если мобильная плита используется в небольшой палатке без вентиляции (вентиляция — это входящий свежий воздух и выходящий дым). Многие люди умерли от отравления угарным газом. Отравление угарным газом может вызывать чувство паранойи и галлюцинации, и было определено, что оно является основной причиной появления домов с привидениями.Небольшие его количества содержатся в угольном газе, топливе, получаемом при нагревании угля без использования воздуха.
Несмотря на то, что это яд, окись углерода очень полезна в химической промышленности, поэтому было обнаружено множество способов ее получения. [2] Обычно мы сжигаем кокс при высоких температурах и недостатке кислорода. Так работают доменные печи. Химическое уравнение для этого:
- 2C + O 2 → 2CO
Его также можно получить путем продувки горячим паром через раскаленный крошеный кокс
- C + H 2 O → CO + H 2
Окись углерода может использоваться в качестве топлива для обогрева, поскольку она легко сгорает до двуокиси углерода.Его также можно использовать в качестве так называемого «синтез-газа» для производства искусственного бензина в процессе Фишера-Тропша.
Во время Второй мировой войны, когда бензин был редкостью и предназначался для военных, многие автомобили были переоборудованы для использования древесного газа . Это окись углерода, образующаяся при сжигании древесной щепы в недостаточном количестве воздуха. Древесный газ производился в специальной печи под названием , генератор , которую перевозили в автомобиле. Полученный окись углерода затем использовалась в качестве топлива для самого автомобиля.Даже сегодня есть автомобили, которые используют древесный газ в качестве топлива.
.Отравление угарным газом может убить
Щелкните здесь, чтобы узнать больше об окиси углерода Поверенный Гордон Джонсон
Отравление угарным газом может убить
Заголовки делают заголовки о смерти от угарного газа. CO чаще всего убивает, лишая сердце кислорода, заставляя сердце перестать биться. Если сердце не будет перезапущено в считанные минуты, наступит смерть. Но смерть — не единственный вид повреждения сердца, который может произойти в результате отравления угарным газом. CO может вызвать несмертельные сердечные приступы и другие сердечные заболевания.Слишком часто СО не учитывается при дифференциальной диагностике во многих из этих ситуаций, особенно у людей, которые в любом случае могли подвергаться риску сердечных заболеваний.
Щелкните здесь, чтобы узнать о симптомах и лечении отравления угарным газом
Источники отравления угарным газом
Наше обращение на Carbonmonoxide.com в первую очередь будет сосредоточено на том, как отравление угарным газом происходит в помещении. Мы начнем с того, что может пойти не так с печами, водонагревателями и духовками, что приведет к выбросу CO в воздух в помещении.На этой странице также будет подробно обсуждаться факторы риска отравления CO при работе бензиновых двигателей в помещениях, в том числе в гаражах. Самый большой виновник в этой сфере — электрические генераторы. CO может также возникать на лодках или рядом с ними, в автомобилях и самолетах.
Окись углерода из печей и водонагревателей
Первый ключ к пониманию воздействия CO состоит в том, что в целом CO является результатом неполного сгорания топлива на основе углерода, такого как нефть и газ, даже древесины и древесного угля.Как правило, устройства для сжигания топлива, такие как печи, печи, водонагреватели и осушители газа, должны гореть достаточно чисто, чтобы CO не был серьезным фактором риска. Значительные уровни CO выбрасываются в воздух только при неисправности этих приборов. Чем больше топлива предназначены для сжигания этих приборов, тем больше вероятность того, что без надлежащей вентиляции утечка CO может произойти в помещении. Под утечкой CO мы подразумеваем выброс этого ядовитого газа в воздух помещения.
Для правильной вентиляции требуется не только отвод выхлопных газов наружу, через дымоход или другую вентиляционную трубу, но и обеспечение достаточного количества кислорода для полного сгорания огня (горения).Таким образом, чем крупнее прибор, тем важнее отводить воздух для горения, которым обычно является наружный воздух. Если есть разрыв или препятствие в выпуске выхлопных газов или в заборе воздуха для горения, может произойти неполное сгорание, что приведет к отравлению угарным газом.
Чтобы лучше понять вопросы взаимосвязи между отрицательным давлением и образованием отравления угарным газом, щелкните здесь.
Отравление угарным газом в гостиницах и школах
Гостиницы являются особенно опасным местом для отравлений угарным газом, потому что там люди спят.Когда воздействие CO происходит посреди ночи, это может привести к летальному исходу, а выжившие часто серьезно отравляются. Хотя CO не так часто приводит к летальному исходу, он также часто поражает школы и офисные здания. В большинстве случаев виноваты старые, плохо обслуживаемые печи и водонагреватели. Мы обсудим каждый из этих типов событий более подробно на наших следующих страницах.
Как CO возникает в отелях?
Что так пугает в мероприятиях с CO в гостиницах, так это то, что, поскольку симптомы имитируют грипп, многие просто засыпают и никогда не просыпаются.Многие из этих отравлений происходят из-за того, что старые котельные системы находятся в плохом состоянии. Проблема становится еще более серьезной, когда франчайзинговые отели первой линии продаются сетям второго уровня, когда здания и бизнес находятся в ведении тех, кто не имеет большого опыта в сфере гостеприимства и управления зданиями. Обогреватели бассейнов также являются серьезным виновником в отелях. Детекторы CO могут спасти жизни, но только если эти детекторы находятся там, где люди слышат, как они срабатывают посреди ночи. Для получения дополнительной информации нажмите здесь.
Насколько серьезна проблема CO в школах?
За последние несколько лет было зарегистрировано три серьезных случая заболевания CO. Группа закона о травмах мозга представляет более 40 человек, отравленных в результате этих событий. Для получения дополнительной информации нажмите здесь.
Воздействие окиси углерода в офисных зданиях?
События CO в офисном здании аналогичны тем, что проводятся в школах. Хотя уровни могут достигать смертельных уровней, потому что несколько человек заболевают почти одновременно, обычно кто-то звонит в службу 911 и эвакуация происходит до того, как они станут смертельными.Но такого рода отравления могут происходить день за днем на таких уровнях, которые не приводят к заболеванию. Для получения дополнительной информации о хроническом отравлении CO щелкните здесь. Считается, что до тех пор, пока уровень карбоксигемоглобина не достигнет 20%, большинство людей не будет рвать или потерять сознание. Очевидно, что повреждение мозга начинает происходить у значительной части тех, кто подвергся воздействию на 10% -ном уровне. Чтобы узнать больше о CO в офисных зданиях, щелкните здесь.
Симптомы угарного газа включают головную боль, тошноту и головокружение
Симптомы, которые часто тревожат людей при наличии CO, — это головные боли, тошнота, рвота и головокружение.К сожалению, многие из ранних симптомов отравления угарным газом напоминают грипп или другое вирусное заболевание. Когда несколько человек отравляются одновременно, часто кто-то теряет сознание и предупреждает о том, что с окружающей средой что-то не так. Когда второй человек заболевает примерно так же, как и другие, менее затронутые люди часто понимают, что происходит нечто иное, чем грипп. Слишком часто люди, страдающие отравлением угарным газом, думают, что страдают от пищевого отравления. Это может произойти, даже если отравились сразу несколько человек, потому что они, возможно, ели одну и ту же пищу.В любом случае следует позвонить в службу экстренной помощи и сначала исключить присутствие окиси углерода. Служба быстрого реагирования должна иметь точные детекторы CO. В случае подозрения на воздействие угарного газа немедленно выйдите на улицу. Не ждите первых откликов.
.Окись углерода — Sciencemadness Wiki
Структура окиси углерода, демонстрирующая тройную связь между атомами углерода и кислорода. | |
| Имена | |
|---|---|
| Название ИЮПАК Окись углерода | |
| Другие наименования Оксид углерода | |
| Недвижимость | |
| CO | |
| Молярная масса | 28.010 г / моль |
| Внешний вид | Бесцветный газ |
| Запах | Без запаха |
| Плотность | 789 кг / м 3 (жидкость) 1,250 кг / м 3 (0 ° C, 1 атм) 1,145 кг / м 3 (25 ° C, 1 атм) |
| Точка плавления | -205,02 ° С (-337,04 ° F, 68,13 К) |
| Температура кипения | -191,5 ° С (-312,7 ° F, 81,6 К) |
| 27.6 мг / л (25 ° С) | |
| Растворимость | Растворим в ледяной уксусной кислоте, водн. аммиак, бензол, хлороформ, водн. HCl-CuCl, этанол, этилацетат, конц. HCl, метанол |
| Давление пара | 1,55 · 10 8 мм рт. Ст. При 25 ° C |
| Термохимия | |
| 197,7 Дж · моль −1 · K −1 | |
| -110,5 кДж / моль | |
| Опасности | |
| Паспорт безопасности | Sigma-Aldrich |
| Температура вспышки | −191 ° С (−311.8 ° F; 82,1 К) |
| Летальная доза или концентрация ( LD , LC ): | |
| 8636 ppm (крыса, 15 мин) 5207 ppm (крыса, 30 мин) 1784 ppm (крыса, 4 часа) 2414 ppm (мышь, 4 часа) 5647 ppm (морская свинка, 4 часа) | |
| Родственные соединения | |
Родственные соединения | Двуокись углерода |
| Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки Infobox | |
Окись углерода представляет собой неорганическое химическое соединение с химической формулой CO , бесцветный газ без запаха, который очень токсичен почти для всех высших форм жизни. Несмотря на присущую ему опасность, это очень полезный и интересный реагент.
Недвижимость
Химическая промышленность
Окись углерода горит при воспламенении в присутствии кислорода с образованием двуокиси углерода.При высоких температурах и давлениях он реагирует с металлами, образуя карбонилы металлов. В органическом синтезе монооксид углерода является обычным методом карбонилирования различных соединений в присутствии металлического катализатора. Он может реагировать с алкенами с образованием карбоновых кислот, его гидрогенизация дает метанол. Как и углерод, при высоких температурах он может восстанавливать оксиды металлов до их элементарной формы.
Физическое
Окись углерода — это остро токсичный газ без цвета и запаха при комнатной температуре.Обнаружить без специального оборудования очень сложно.
Наличие
Окись углерода — обычное промышленное химическое вещество, но маловероятно, что частные лица могут легко получить его, учитывая его токсичность. Обычно его нужно приготовить в лаборатории. Оно также может образоваться (крайне нежелательно и опасно для жизни человека), когда некорректно топят дровяную или угольную печь, или держат автомобиль с работающим двигателем в закрытом гараже.
Препарат
Окись углерода чаще всего образуется в результате неполного сгорания органических материалов, которое происходит без достаточного количества кислорода.Тем не менее, его чаще всего производят для лабораторного использования путем дегидратации муравьиной кислоты или щавелевой кислоты с использованием концентрированной серной кислоты. Его также можно приготовить в нечистой форме, пропустив воздух или кислород через горящий кокс или древесный уголь, а затем еще раз через горячий, но негорючий древесный уголь, включая летучие соединения и диоксид углерода в качестве примесей. Прохождение углекислого газа через раскаленный уголь также дает окись углерода. Пропускание водяного пара через раскаленный уголь или добавление к нему воды приведет к образованию легковоспламеняющейся смеси монооксида углерода и газообразного водорода, известной как «водяной газ», тип синтез-газа.
- H 2 O + C → H 2 + CO (ΔH = +131 кДж / моль)
Окись углерода также может быть получена путем нагревания эквимолярной смеси карбоната кальция и порошка цинка:
- CaCO 3 + Zn → CaO + ZnO + CO
Поскольку оксид углерода без запаха и очень токсичен, лучше не производить оксид углерода в высоких концентрациях без надлежащего оборудования и защиты, и определенно не производить вообще, если у вас нет любой опыт. Наличие исправного детектора угарного газа обязательно.
Проектов
Обработка
Безопасность
Окись углерода очень токсична и может легко потерять сознание из-за кислородного голодания. Если человека, выведшего из строя таким образом, быстро не вывести из окружающей среды, содержащей окись углерода, смерть почти неизбежна. Симптомы отравления угарным газом очень легко игнорировать. Нужно быть очень осторожным, используя или пытаясь сохранить окись углерода; определенно рекомендуется использовать его только на улице (вытяжного шкафа может быть недостаточно, но если его необходимо использовать, то датчик угарного газа — хорошая идея).Безответственные действия с этим химическим веществом представляют угрозу не только для вас самих, но и для всех, кто находится поблизости, поэтому дважды подумайте, прежде чем использовать его.
В случае отравления угарным газом пациенту следует немедленно покинуть зараженное помещение (или быть перенесенным оттуда) и получить доступ к наружному воздуху. В случае сильного отравления пациенту следует немедленно обратиться за медицинской помощью. Если медицинская помощь недоступна, пациенту следует дать чистый кислород для дыхания и внутривенно ввести метиленовый синий, который является общим противоядием против агентов крови, которые атакуют гемоглобин или цитохромоксидазу; дозировка — 50-100 мл 1% раствора.Другие антидоты против окиси углерода включают кобинамид и ацизол (российский антимоноксид).
Хранилище
Хранение окиси углерода в виде сжатого газа и карбонильных соединений опасно, так как в случае утечки CO будет подниматься и хорошо рассеиваться в воздухе (поскольку его молярная масса аналогична молярной массе азота. Детектор окиси углерода должен быть используется в непосредственной близости от любого потенциального выброса любого размера.
Утилизация
Окись углерода должна выделяться в воздух только при отсутствии риска накопления.
Список литературы
Соответствующие темы Sciencemadness
.Окись углерода — молекула месяца
Окись углерода — молекула месяца — ноябрь 2005 г. Доктор Майк Томпсон
Винчестерский колледж, Великобритания
Молекула месяца — ноябрь 2005 г.
Также доступны версии Chime Enhanced, VRML и JMol.
Окись углерода — это токсичный газ без цвета и запаха.Он был неоценим, помогая химикам извлекать металлы из руд. Однако следует сказать, что его физические свойства делают его потенциально очень опасным.
Производство окиси углерода
Углерод и кислород могут образовывать два газа. Когда сгорание углерода завершено, , т.е. . в присутствии большого количества воздуха продукт представляет собой в основном двуокись углерода (CO 2 ). Источники углерода включают; уголь, кокс, древесный уголь. При неполном сгорании углерода i.е . подача воздуха ограничена, к углероду добавляется только половина кислорода, и вместо этого образуется окись углерода (CO).
Окись углерода также образуется в качестве загрязнителя при сжигании углеводородного топлива (природного газа, бензина, дизельного топлива). Относительное количество произведенного CO зависит от эффективности сгорания. Старые автомобили ежегодно проверяются на выбросы CO во время теста MOT. Интересно, что только один из двух оксидов углерода не поддерживает горение, и именно по этой причине диоксид углерода используется в огнетушителях.Окись углерода поддерживает горение и горит бледно-голубым пламенем. Голубое пламя раньше видели над кострами, сделанными из кокса (по сути, очень чистой формы углерода) ночные сторожа на промышленных объектах.
2 CO (г) + O 2 (г) 2 CO 2 (г)
Лабораторное приготовление окиси углерода
Из углерода:
При производстве окиси углерода необходим источник углекислого газа.Это может быть баллон с CO 2 или даже сухой лед (твердый CO 2 ). Если ни один из них не доступен, диоксид углерода может быть образован реакциями нейтрализации между кислотой и карбонатом или кислотой и гидрокарбонатом.
2HCl (водн.) + CaCO 3 (т) CaCl 2 (водн.) + H 2 O (л) + CO 2 (г)
HCl (водн.) + NaHCO 3 (т) NaCl (водн.) + H 2 O (л) + CO 2 (г)
При пропускании углекислого газа над нагретым древесным углем образуется окись углерода.
CO 2 (г) + C (т) 2CO (г)
Также будет непрореагировавший диоксид углерода, который необходимо удалить. Двуокись углерода удаляют путем реакции с водным раствором гидроксида натрия.
2 NaOH (водн.) + CO 2 (г) Na 2 CO 3 (водн.) + H 2 O (л)
Из метановой кислоты:
Еще один удобный способ получения окиси углерода — дегидратация метановой кислоты с использованием конц.Н 2 СО 4 .
HCOOH (водн.) CO (г) + H 2 O (л)
Обезвоживание метановой соли, такой как метаноат натрия, также хорошо работает. В этом случае вы капаете концентрированную серную кислоту прямо на твердое вещество. Выделяющийся окись углерода может собираться под водой. Метановая кислота содержится в крапиве и муравьях.
Насколько ядовит?
Окись углерода — очень ядовитый газ.Он ядовит при уровне всего 0,1% (1000 частей на миллион). Его токсичность возникает из-за его способности связываться с переходными металлами, такими как железо, находящееся в центре молекулы гема. Окись углерода притягивается к гемоглобину более чем в 200 раз сильнее, чем кислород. Таким образом, присутствие в крови окиси углерода препятствует тому, чтобы часть гемоглобина, содержащегося в красных кровяных тельцах, переносила достаточное количество кислорода.
Этот факт, безусловно, стоит учесть, если у вас возникнет соблазн выкурить сигарету.Было обнаружено, что у курильщиков довольно высокий уровень окиси углерода в крови спустя много времени после того, как они закурили выбранную сигарету.
Симптомы отравления угарным газом — головокружение и головные боли. Эти страдания можно спутать с другими заболеваниями, например с гриппом. Отравление угарным газом можно распознать, так как жертвы часто имеют неестественно яркие красные губы.
Продолжительное воздействие окиси углерода может в конечном итоге привести к смерти.Окись углерода использовалась как яд при самоубийствах. Еще более тревожным было использование нацистами окиси углерода во время Второй мировой войны для убийства своих жертв в лагерях смерти. Совсем недавно были случаи, когда арендодатели-мошенники не обслуживали газовые приборы должным образом, что приводило к гибели арендаторов, зачастую студентов. Закон в Великобритании теперь требует ежегодной проверки котлов, газовых плит и газовых каминов зарегистрированными инженерами. Следующее уравнение показывает, что происходит при неполном сгорании природного газа, в основном метана.
2 CH 4 (г) + 3 O 2 (г) 2 CO (г) + 4 H 2 O (г)
Уголь газ
До того, как под морями и океанами были обнаружены огромные количества природного газа, мы сжигали угольный газ. Угольный газ производился при нагревании угля в отсутствие воздуха. Его основные компоненты — водород, метан и окись углерода.
Окись углерода иногда встречается в угольных шахтах. Одно время канарейки вырубали в шахтах для обнаружения ядовитых газов.Канарейки будут убиты в дозах, не смертельных для шахтеров. Сегодня газы более гуманно обнаруживаются приборами.
Восстановитель
Большинство студентов впервые сталкиваются с угарным газом на уроке химии при его использовании в доменной печи. В доменной печи железо извлекается из руды, гематита (оксид железа (III) Fe 2 O 3 ).
Fe 2 O 3 (т) + 3 CO (г) 2 Fe (л) + 3 CO 2 (г)
Окись углерода является сильным восстановителем и восстанавливает оксиды металлов для металлов, менее активных, чем углерод.Следующая таблица полезна для различных определений редукции. Поскольку окисление противоположно восстановлению, вам нужно усвоить только половину фактов!
| Восстановление | Окисление |
|---|---|
| Потеря кислорода | Прирост кислорода |
| Прирост водорода | Потеря водорода |
| Прирост электронов | Уменьшение количества электронов | Уменьшение .№ | Увеличение O.N. |
Реакции окиси углерода
Несколько газов (H 2 , CH 4 и CO) исторически использовались в качестве восстановителей. Одно из определений восстановителя, которое мне особенно нравится, — это думать о нем как о захвате кислорода. Важно помнить, что окисляется сам восстановитель. Быстрое и простое лабораторное восстановление может быть достигнуто путем нагревания смеси черного оксида меди (II) с углеродным порошком в пробирке.После нескольких минут нагревания сбоку пробирки можно увидеть красноватую медь. По сути, углерод действует как восстановитель, а также как монооксид углерода, который неизбежно образуется при его нагревании на воздухе. В этом простом эксперименте происходят следующие реакции.
CuO (тв) + CO (г) Cu (тв) + CO 2 (г)
CuO (тв) + C (тв) Cu (тв) + CO (г)
C (т) + O 2 (г) 2 CO (г)
C (т) + O 2 (г) CO 2 (г)
CO 2 (г) + C (т) 2 CO (г)
Сродство к переходным металлам
Окись углерода не проявляет кислотных или основных свойств.Его слабая кислотность по Льюису проявляется в образовании H 3 BCO с бораном (BH 3 ). Окись углерода обладает замечательным сродством к переходным металлам (находится между 2 и 3 группами Периодической таблицы). Первые образцы карбонилов металлов появились еще в 1888 году, когда были получены и охарактеризованы тетракарбонил никель (0) Ni (CO) 4 и пентакарбонил железа (0) Fe (CO) 5 . Бывший комплекс является частью Мондовского процесса по очистке никеля.Ni (CO) 4 перегоняется с получением чистого никеля.
Ni (тв) + 4 CO (г) Ni (CO) 4 Ni (тв) + 4 CO (г)
Окись углерода настолько реактивна с никелем, что в течение нескольких минут протравит поверхность. Ni (CO) 4 очень токсичен с затхлым запахом. Этот тетраэдрический комплекс не только горюч, но и легко разлагается на составляющие. Окись углерода действует как лиганд по отношению к переходному металлу через неподеленную пару на атоме углерода.Двухатомный оксид углерода имеет тройную связь между своими атомами. Одна из связей, образующих тройную связь, является дательной ковалентной связью.
Попробуйте это дома
В наши дни обнаружение окиси углерода — простая задача. В большинстве хозяйственных магазинов продаются специальные пятна, пропитанные соединениями палладия, которые темнеют под воздействием окиси углерода.
Вернуться на страницу «Молекула месяца». [DOI: 10.6084 / m9.figshare.5436793]
.